製薬業界/GMP・バリデーション・電子記録・電子署名・PART11対応
GMPを意識した生産管理システム構築のポイント

GMPを意識した生産管理システム構築手順
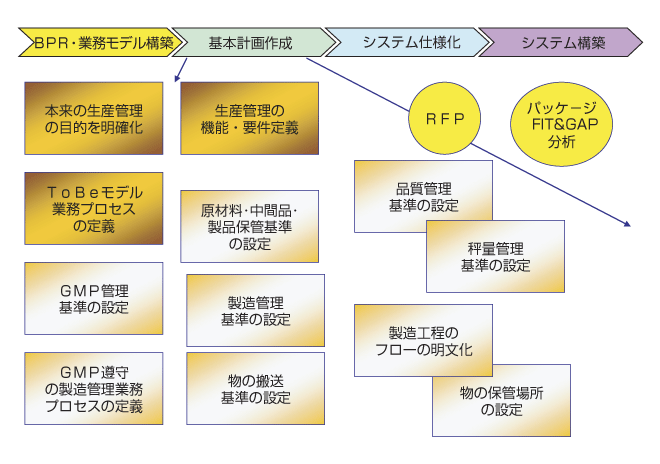
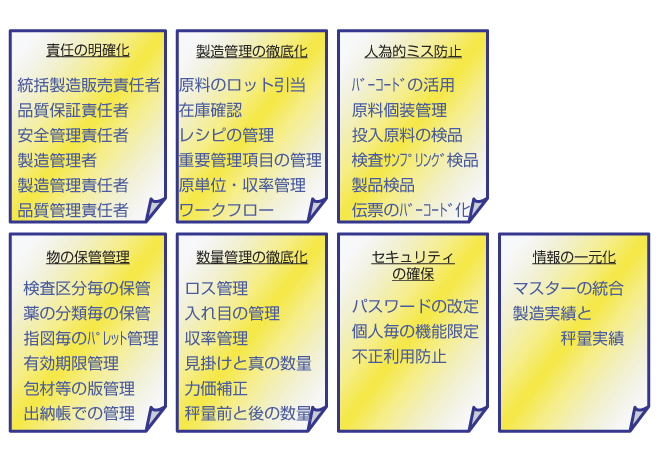
GMPを意識した生産管理システム構築の考慮点
コンピュータバリデーションのご支援
1)バリデーション支援
サービス・機器・プロセス・洗浄等を含む医薬品製造における全ての面で一貫して適正に機能することを高度に文章で保証する必要がありますが、当然システムにおいても必要です(コンピュータバリデーション CSV)
2)予測的バリデーション(実生産バリデーションを含む)
開発されたシステムが、当初意図したように適正に作動することを実証
3)同時的バリデーション
製造する日常の中で、システムが適正に作動していることを実証
4)変更時の再バリデーション
システムの変更を生じた場合、必要と思われる対象範囲に再度バリデ-ションを実施
5)回顧的バリデーション
過去のデータを統計的手段によって正しく作動したことを実証
コンピュータバリデーションを前提とした生産管理システム構築手順
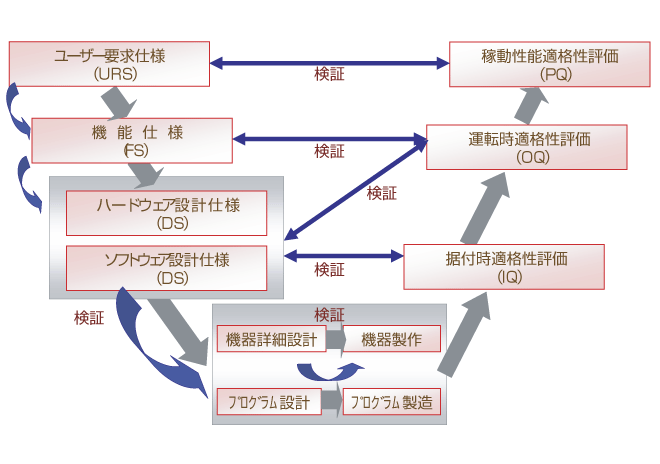
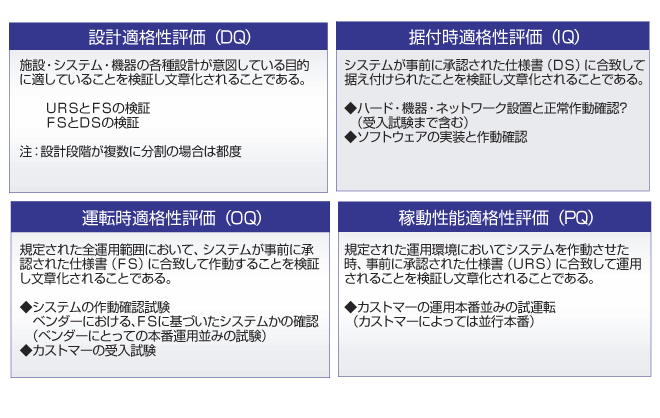
適格性評価のポイント
製薬業界にとってのPART11(電子承認・電子記録)の重要性
1)PART11への弊社のスタンス
- 単にPart11のみを考えるのではなく、GMP、コンピュータバリデーション、Part11の3つを同時に考えていく事が重要
- コンピュータバリデーションが、Part11を考えるにあたっての絶対的条件
- 電子記録と手書き記録および電子承認と手書き承認を混在させたハイブリッドシステムが前提
2)PART11導入のメリット
- SOX法、国際会計基準IFRSというグローバルスタンダードの流れと同じ思想の一つであり、医薬の海外展開する上で重要な課題
- 製薬業界は、もっと自動化・システム化を図り、世界に打ち勝つ体質改善を求められている。しかし一方情報化の危険・リスクも増加しており、その危険を回避するためにも必要な課題
PART11対象の電子記録
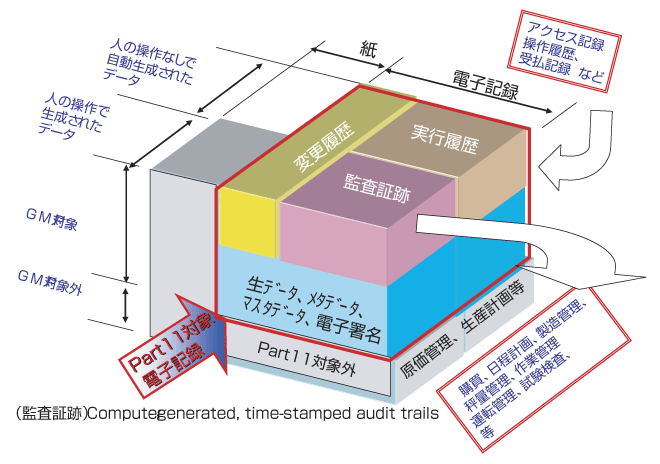
PART11として考えねばならないメニュー
1)電子記録の対象および電子署名の宣言
手書き記録・監査証跡・変更履歴・実行履歴・電子署名等
2)システム利用者の限定
個人の身元保証・利用権の設定・パスワードの改変等
3)システム利用環境の限定
クローズ/オープンシステム・デバッグチェック・外部会社との接続等
4)アクセス権と不正アクセスの管理
権限チェック・アクセス権の失効・離籍対応・操作と実行履歴等
5)電子署名とその管理
署名権限・署名理由・代理人署名・連続署名等
6)電子記録の課題と対応
信憑性・一貫性・再現性・コピー情報の改竄防止の実現等
7)タイムスタンプと監査証跡
8)コンピュータバリデーション
9)システムの保全性